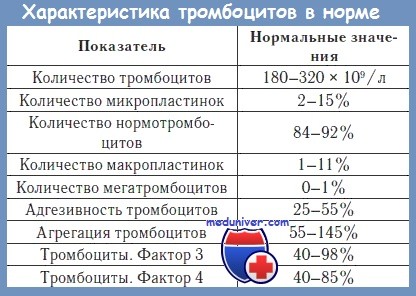
Адгезия тромбоцитов что это
Морфологическое исследование тромбоцитов: примерная численность, величина, аспект, распределение. Количественное: счисление тромбоцитов. Качественное исследование тромбоцитов: функциональность, подразделяющаяся на: динамическую, определяемую способами адгезивности, аггрегации и ретракции плазматического сгустка; тромбопластическую, выявляемую определением активности тромбоцитного фактора 3, ТРП, ТОТ.
Способы исследования адгезивности тромбоцитов можно разделить на методы в пробирке и прижизненные методы.
Принцип обеих методов одинаков: измерение сокращения числа тромбоцитов крови, вступающей в контакт с посторонней поверхностью, в течение стандартного срока.
Тест Borchgreving составляет прижизненный способ исследования и заключается в измерении расхода тромбоцитов у стандартного надреза кожи.
Тест Зальцмана состоит в прохождении свежей, как таковой или гепаринизированной венозной крови, равномерным объемным потоком через стандарную колонку со стеклянными шариками. Разность числа тромбоцитов до и после прохождения через стеклянные шарики составляет число, задержанных в колонке тромбоцитов.
Адгезивность уменьшается при отдельных тромбопатиях, болезни Виллебранда, афибриногенемиях и дефиците фактора XII.
Адгезивность повышается при тромбозе.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Этот загадочный тромбоцит
Алена Якименко, Анастасия Свешникова, Елена Артеменко, Михаил Пантелеев
«Природа» №2, 2014
Об авторах
Алена Олеговна Якименко (вторая слева) — кандидат биологических наук, старший научный сотрудник Центра теоретических проблем физико-химической фармакологии (ЦТПФХФ) РАН. Область научных интересов — свертывание крови, механизмы тромбообразования, субпопуляции активированных тромбоцитов крови человека.
Анастасия Никитична Свешникова (крайняя справа) — кандидат физико-математических наук, старший научный сотрудник физического факультета МГУ им. М. В. Ломоносова. Научные интересы связаны с компьютерным моделированием биологических процессов, изучением внутриклеточной сигнализации, биохимии свертывания крови.
Елена Олеговна Артеменко — научный сотрудник ЦТПФХФ РАН. Занимается исследованием реорганизации цитоскелета тромбоцитов при активации и механизмов, приводящих к формированию прокоагулянтных активированных тромбоцитов.
Михаил Александрович Пантелеев — доктор физико-математических наук, профессор, заведующий лабораторией молекулярных механизмов гемостаза ЦТПФХФ РАН. Лауреат премии им. Р. В. Хохлова (2002) и премии Европейской академии (2007). Область научных интересов — механизмы регуляции гемостаза и тромбоза, биохимия и биофизика свертывания крови, математическое моделирование биологических систем.
Важнейшую роль тромбоцитов в живом организме открыл итальянский врач и патолог Джулио Биццоцеро, который в 1882 г. провел ряд блестящих экспериментов, имея в своем распоряжении лишь световой микроскоп. Сегодня у нас куда больше измерительных приборов и вычислительных машин, выполняющих сложнейшие математические расчеты, однако множество вопросов остаются открытыми. Известно, что тромбоциты играют ключевую роль в остановке кровотечения из раны (гемостазе * ) и опасном перекрывании здорового сосуда (тромбозе). Однако до сих пор неясно, как именно функционирует система гемостаза. Какие причины приводят к ее переключению с защиты организма на развитие угрожающих жизни патологий? Какова роль тромбоцитов в регуляции процессов гемостаза и тромбоза? Не знаем мы, и зачем тромбоциты устроены так сложно, и не представляем всю последовательность событий, обеспечивающих формирование тромба в месте повреждения, а экспериментальные данные приносят с собой новые загадки.
Строение
Рис. 1. Микрофотография неактивированных тромбоцитов [1]
Тромбоциты (от греч. θρομβοζ — ‘сгусток’ и κυτοζ — ‘клетка’) — специализированные безъядерные клетки крови, имеющие форму диска диаметром около 3 мкм и толщиной около 0,5 мкм (рис. 1). Образуются они при фрагментации больших клеток костного мозга — мегакариоцитов и циркулируют в кровотоке в концентрации 200–400 тыс. клеток в 1 мкл крови. Живут тромбоциты в кровотоке в среднем 5–9 дней, а затем разрушаются в селезенке и печени.
Устроен тромбоцит довольно сложно. Снаружи он ограничен билипидным слоем мембраны, многочисленные впячивания которой (открытая канальцевая система) дают запас поверхности для изменения формы (рис. 2). Поддерживает ее и одновременно позволяет сильно менять цитоскелет (каркас) клетки. Внутри находятся эндоплазматический ретикулум (хранилище ионов кальция, необходимых для сигнализации и выполнения тромбоцитом своих функций) и митохондрии (органеллы, обеспечивающие дыхание). В цитозоле присутствуют гранулы, содержащие вещества, выплескивающиеся при активации клетки (переходе в новое состояние) во внеклеточное пространство. В плотных гранулах содержатся нуклеотиды (АТФ, АДФ, ГТФ, ГДФ), серотонин, ионы кальция в высокой концентрации, в α-гранулах — различные белки (в том числе факторы свертывания крови), а в лизосомах — некоторые ферменты (коллагеназа, эластаза и др.).

Рис. 2. Схема строения тромбоцита [2]
После активации тромбоцита на внешней поверхности его мембраны появляется отрицательно заряженный липид — фосфатидилсерин. С ним с помощью ионов кальция связываются некоторые факторы свертывания, формируя специальные комплексы. Они во много раз ускоряют реакции, приводящие к желированию плазмы крови у места повреждения (этот процесс называется плазменным гемостазом). Иными словами, фосфатидилсерин обеспечивает прокоагулянтную, способствующую плазменному гемостазу, функцию тромбоцитов.
Почему же век этих клеток крови столь недолог (эритроциты, например, живут три-четыре месяца), ведь в норме, в отсутствие серьезных повреждений сосудов, они практически не работают? Почему они имеют вид дисков? Зачем тромбоциту митохондрии, если его энергетические расходы крайне скромны? Зачем природе понадобилось ускорять реакции плазменного свертывания на клеточных мембранах? Для чего α-гранулы содержат белки свертывания, которые есть и в плазме крови? Это только некоторые из вопросов, не имеющих пока четких ответов.
Активация
Для выполнения своей основной функции — заделывания повреждения в стенке сосуда — тромбоциты должны перейти в активное состояние. Как и у большинства клеток нашего организма, этот процесс протекает по следующей схеме: сигнал — рецептор — внутриклеточный сигнал — усилитель — регулятор — ответ (рис. 3). Сигналом к активации служит появление в кровотоке агониста — специальной сигнальной молекулы, которая должна появляться только при необходимости и связываться со специфической молекулой, пронизывающей мембрану тромбоцита (рецептором). Агонист взаимодействует с одним «хвостом» рецептора, выступающим снаружи, и это приводит к изменению другого, со стороны цитозоля, где появляется следующая сигнальная молекула — вторичный мессенджер. Он запускает синтез еще нескольких мессенджеров, те, в свою очередь, — еще нескольких, и так сигнал распространяется в цитозоле и усиливается с помощью каскада внутриклеточных реакций, что в конечном итоге приводит к комплексному ответу тромбоцита. Важно, что в тромбоците существуют специальные регуляторные системы, модулирующие концентрации внутриклеточных мессенджеров на разных этапах активации, чтобы, например, не было реакции на следовые количества агониста.
Рис. 3. Схема активации тромбоцита
Как же эта схема реализуется в нашем организме? В сосудах тромбоциты выталкиваются эритроцитами из основного потока и движутся вдоль стенок, проводя своего рода мониторинг их состояния. Одним из первых сигналов к активации тромбоцитов становится коллаген — основной белок соединительной ткани, обнажающийся при повреждении сосуда. Обнаружив коллаген, они связываются с ним через специальные рецепторы, одновременно активируясь и прочно прикрепляясь к месту повреждения. Взаимодействие тромбоцита с коллагеном и ведет к запуску упомянутого внутриклеточного сигнального каскада и появлению в цитозоле вторичного мессенджера — инозитолтрифосфата (ИФ3). Эта маленькая водорастворимая молекула способна быстро передвигаться в цитозоле и служит сигналом к выходу ионов кальция из внутриклеточных хранилищ. А повышение его внутриклеточной концентрации может приводить к разнообразным ответам тромбоцита: выплескиванию содержимого гранул (секреции), изменению формы, прикреплению к стенке сосуда (адгезии), скреплению с другими тромбоцитами (агрегации), появлению прокоагулянтной активности (рис. 4). После того, как кровеносная система уже распознала повреждение сосуда, в крови появляются еще три природных активатора тромбоцита — тромбин, АДФ и тромбоксан A2. Белок тромбин образуется из предшественника, протромбина, в плазме крови, но массово — уже на мембранах активированных тромбоцитов. При секреции их плотных гранул выбрасывается большое количество АДФ (маленькая молекула, выполняющая в клетках в основном энергетические функции), и гораздо меньше АДФ высвобождается из поврежденных клеток эндотелия, выстилающего внутреннюю поверхность сосудов. Из арахидоновой кислоты, находящейся в мембранах активированных тромбоцитов, синтезируется тромбоксан А2. Связывание этих трех активаторов со своими рецепторами на мембране тромбоцита приводит, как и в случае с коллагеном, к появлению ИФ3 в цитозоле и повышению в нем концентрации кальция (рис. 4). Таким образом, все три растворимых активатора и коллаген действуют по одному пути, однако вызывают разные тромбоцитарные ответы. Например, тромбоксан А2 провоцирует выброс плотных гранул, а АДФ — нет. Активация отдельно коллагеном или тромбином вызывает все перечисленные ответы одновременно, а совместно — приводит к появлению группы прокоагулянтных тромбоцитов и синтезу тромбина на их мембранах. Видимо, существуют еще недостаточно изученные различия в сигнализации, запускаемой разными агонистами. Чтобы случайная активация не превращала тромбоцит в настоящую «бомбу», несущуюся в кровотоке и запускающую всю систему свертывания, в организме неповрежденные клетки эндотелия постоянно выделяют простациклин и оксид азота, которые блокируют активацию клеток, препятствуя повышению в них концентрации кальция.
Рис. 4. Схема основных путей активации тромбоцита и его ответных реакций: АДФ — аденозиндифосфат, ИФ3 — инозитолтрифосфат, ЭПР — эндоплазматический ретикулум
Сигнализация — один из самых сложных и плохо изученных разделов в исследовании тромбоцитов. По устройству каждого рецептора и сигнального пути существует множество вопросов, и самый простой из них: зачем вообще столько активаторов?
Цитоскелет и изменение формы
Цитозоль тромбоцита пронизан трехмерной сетью из водонерастворимых белковых нитей (филаментов), которая формирует цитоскелет. Филаменты состоят из полимеризованного белка актина и обеспечивают изменение формы тромбоцита при активации. Кроме того, непосредственно под плазматической мембраной находится мембранный скелет, связанный с цитоплазматическими «хвостами» некоторых рецепторов. Состоит он из коротких актиновых филаментов, соединенных друг с другом с помощью специальных белков. Мембранный скелет не только поддерживает плазматическую мембрану, регулируя контуры клетки, и стабилизирует ее, предотвращая фрагментацию, но и регулирует распределение в плоскости мембраны рецепторов, прикрепленных к нему. Также предполагают, что он играет важную роль в регуляции различных внутриклеточных событий, которые запускаются при активации.
Рис. 5. Сканирующие электронные микрофотографии процесса распластывания активированного тромбоцита (а–г) по поверхности [3]
Интересно, что цитоскелет — структура динамичная, благодаря которой тромбоцит может не только менять форму, но и отращивать «щупальца» (филоподии). С их помощью он распластывается по поверхности поврежденного сосуда (рис. 5) и легче прилепляется к другим тромбоцитам (рис. 6). Относительно недавно было обнаружено, что при сильной активации (одним тромбином или вместе с коллагеном) тромбоциты разделяются на две группы (субпопуляции), сильно отличающиеся по свойствам и даже форме, что предполагает принципиально разную организацию в них цитоскелета. Одни из них («обычные» активированные) имеют вид амеб — комков с филоподиями, другие (прокоагулянтные, так как на внешней поверхности их мембраны много фосфатидилсерина) — шариков без «щупалец». Полученные в нашей лаборатории данные свидетельствуют о том, что некоторые мембранные рецепторы, отвечающие за связывание клеток с поверхностью и друг с другом, у тромбоцитов из двух субпопуляций неодинаково прикреплены к цитоскелету. А это значит, что они могут по-разному взаимодействовать с поврежденной сосудистой стенкой и друг с другом в формирующемся тромбе.
Последовательность процессов при перестройке цитоскелета тромбоцита вообще изучена пока достаточно мало, а тут уже новый вопрос: зачем одним клеткам при активации становиться «амебами», а другим — «шариками»?
Адгезия и агрегация
Рис. 6. Сканирующая электронная микрофотография агрегата тромбоцитов [4]. Увел. ×11,5 тыс.
Чтобы залатать неисправный сосуд и предотвратить кровопотерю, тромбоцитам нужно прикрепиться к месту «аварии» (адгезия) и друг к другу (агрегация). Первые обнаружившие повреждение клетки прикрепляются к нему и формируют нижний слой тромба. К ним прилепляются новые тромбоциты из потока, и постепенно образуется тромбоцитарный агрегат (рис. 6). Но между клетками в нем остаются промежутки, через которые может просачиваться плазма крови, поэтому она желируется вблизи места повреждения в результате реакций между факторами свертывания. Образующийся гель заполняет промежутки между тромбоцитами и полностью останавливает вытекание крови из раны. Адгезия и агрегация в норме ведут к перекрыванию места «аварии» и предотвращению кровопотери, а при патологических условиях, плохо пока изученных, вызывают формирование тромбов, мешающих нормальному кровотоку в здоровых сосудах. Их тромбирование является причиной многих сердечно-сосудистых заболеваний, в том числе инфарктов и инсультов.
Адгезия происходит за счет связывания специальных рецепторов, гликопротеинов (ГП) VI и Ib и интегрина αIIbβ3 (или ГП IIbIIIa), на мембране тромбоцита с определенными белками на поверхности поврежденного сосуда. Агрегация же происходит за счет ГП Ib и IIbIIIa и представляет собой образование связи между двумя рецепторами посредством растворенного в плазме крови лиганда (от лат. ligare — ‘связывать’; вещество, специфически соединяющееся с рецептором). Гликопротеинам Ib и VI для связывания лигандов не требуется дополнительных условий, в отличие от ГП IIbIIIa, который приобретает такую способность только благодаря своим конформационным изменениям, происходящим после активации тромбоцита. Фибриноген и фактор Виллебранда, основные лиганды интегрина αIIbβ3, обладают симметричной структурой и поэтому взаимодействуют одновременно с двумя рецепторами на соседних активированных тромбоцитах, формируя между ними скрепляющие «мостики» (рис. 4).
Рассмотрим приближенную последовательность событий, происходящих с тромбоцитами при нарушении целостности сосуда. Повреждение эндотелия приводит к выставлению в кровоток коллагена, на который из плазмы крови тут же садятся молекулы фактора Виллебранда. Тромбоциты, приносимые к месту травмы, связываются с ними, а затем с коллагеном через рецепторы ГП Ib и ГП VI соответственно. Это запускает сигнальные процессы, приводящие к активации интегринов αIIbβ3 и к началу формирования тромба. По мере того как клетки склеиваются друг с другом за счет интегринов αIIbβ3, они секретируют тромбоксан А2 и АДФ, которые активируют интегрины αIIbβ3 на проносящихся в потоке тромбоцитах, вовлекая их в растущий тромб.
В нашем организме размеры сосудов и скорости кровотока меняются от аорты с диаметром 2,5 см и средней скоростью потока 48 см/с до мельчайших капилляров диаметром 0,0008 см и скоростью течения крови 0,1 см/с. Тромбоциты обладают уникальной способностью формировать стабильные контакты друг с другом в этом широком диапазоне условий. А удается им это благодаря тому, что при разных условиях вклад различных рецепторов, осуществляющих прикрепление тромбоцитов к стенке сосуда или друг к другу, сильно меняется. И когда работа одного рецептора оказывается неэффективной, инициативу подхватывает другой, лучше приспособленный к данным условиям.
Напомним, что традиционной схемой скрепления двух тромбоцитов является образование связей «рецептор на одной клетке — лиганд в плазме — рецептор на другой». Однако недавно нам удалось показать, что существует еще одна схема — «рецептор на одной клетке — лиганд на другой» [5]. На внешней поверхности мембраны прокоагулянтных тромбоцитов непонятным пока образом удерживается большое количество белков α-гранулярного происхождения, в частности фибриноген и фактор Виллебранда. Из-за этой белковой «шубы» такие тромбоциты некоторое время назывались в литературе «укутанными», при этом интегрины αIIbβ3, основные рецепторы агрегации, на них парадоксальным образом неактивны и не могут связывать свои лиганды. В связи с этим долгое время считалось, что прокоагулянтные тромбоциты вообще не могут агрегировать, однако, как мы выяснили, способны слепляться с «обычными» активированными тромбоцитами (но не друг с другом). И происходит это за счет связывания активных интегринов αIIbβ3 на поверхности «обычных» активированных тромбоцитов и лигандов этого рецептора, удерживаемых на поверхности прокоагулянтных тромбоцитов в составе их белковой «шубы».
Сегодня уже достаточно хорошо известно, как запускается и происходит рост тромба, но неясно, как этот процесс останавливается. Почему в норме рост тромба со временем прекращается, не приводя к закупорке сосуда? Вероятно, ответ на этот вопрос кроется в сложном одновременном действии множества факторов, оказывающих влияние на рост тромба, включая локальные условия кровотока и концентрации растворимых агонистов — таких как АДФ, тромбоксан А2 и тромбин.
Итак, прокоагулянтные тромбоциты по сравнению с «обычными» активированными обладают лучшей способностью ускорять плазменный гемостаз и особым механизмом агрегации — могут скрепляться с «обычными» активированными тромбоцитами, но не с себе подобными. Формирование субпопуляций, обладающих уникальными комбинациями свойств, — один из самых интересных и сложных феноменов в науке о тромбоцитах. Экспериментальных данных, накопленных в результате более 15 лет продолжающихся исследований, достаточно, чтобы предполагать, что субпопуляции этих клеток играют разные роли в регуляции роста тромба. Сейчас в нашей и нескольких зарубежных лабораториях ведется активная работа по выявлению (пато)физиологической роли тромбоцитарных субпопуляций и исследование их пространственного распределения в растущих тромбах. Эти знания позволят разработать новые лекарства, избирательно влияющие на клетки разных субпопуляций. Так мы сможем вмешиваться в регуляцию роста тромба и предотвращать развитие патологических процессов (тромбоза), а там, где это требуется, наоборот, стимулировать нормальный гемостаз.
Тромбоциты обеспечивают остановку кровотечения и одновременно играют главную роль в тромбозе. Постепенно все больше вопросов, связанных с этими клетками, находят ответы, но тромбоциты таят в себе еще очень много секретов. Достаточно добавить, что в последние 20 лет было обнаружено их участие в иммунном ответе, воспалении, регенерации тканей, ангиогенезе (образовании новых кровеносных сосудов) и даже развитии опухолей. Дальнейшее изучение тромбоцитов поможет лучше понять протекание многих жизненно важных процессов нашего организма, но в первую очередь станет решающим шагом в победе над тромбозом — основной причиной смертности в развитых странах.
Работа выполнена при поддержке Программы фундаментальных исследований Президиума РАН «Молекулярная и клеточная биология» и Российского фонда фундаментальных исследований (проекты № 12-04-31401, 12-04-31788, 12-04-31873, 12-04-32246, 12-04-33055, 13-04-00401, 14-04-00670).
Литература
1. Ohlmann P., Eckly A., Freund M. et al. ADP induces partial platelet aggregation without shape change and potentiates collagen-induced aggregation in the absence of Galphaq // Blood. 2000. V. 96. № 6. P. 2134–2139.
2. White J. G. Electron microscopy methods for studying platelet structure and function // Platelets and megakaryocytes / Eds J. M. Gibbins, M. P. Mahaut-Smith. Totowa; N. J., 2004. P. 47–63.
3. Fatisson J., Mansouri S., Yacoubet D. et al. Determination of surface-induced platelet activation by applying time-dependency dissipation factor versus frequency using quartz crystal microbalance with dissipation // J. R. Soc. Interface. 2011. V. 8. № 60. P. 988–997.
4. Gerrard J. M., White J. G., Rao G. H. et al. Effects of the lonophore A23187 on the blood platelets II. Influence on ultrastructure // Am. J. Pathol. 1974. V. 77. № 2. P. 151–166.
5. Yakimenko A. O., Verholomova F. Y., Kotova Y. N. et al. Identification of different proaggregatory abilities of activated platelet subpopulations // Biophys. J. 2012. V. 102. № 10. P. 2261–2269.
* Подробнее см.: Баландина А. Н., Пантелеев М. А., Атауллаханов Ф. И. Система свертывания крови и ее регуляция // Природа. 2011. № 3. С. 32–38 (PDF, 4 Мб).
Адгезия тромбоцитов что это
Кровяные пластинки, безъядерные клетки крови, являются основой первичного гемостаза. Интактные тромбоциты имеют форму гладких двояковыпуклых дисков диаметром 2-5 мкм. Этосамые малые по размерам клетки крови. Плазматическая мембрана тромбоцитов, состоящая из полярных фосфолипидов и белков, имеет толщину 7-8 нм. Углеводородные остатки гликопротеидов и гликолипидов плазматической мембраны образуют внешнюю оболочку клеток, называемую гликокаликсом [3].
У кровяных пластинок большинства видов биологических объектов имеются две дискретные системы мембран: систему открытых каналов и плотную тубулярную систему. Последняя представлена узкими трубочками диаметром около 50 нм, которые на поперечном сечении тромбоцитов могут выглядеть как пу зырьки. Часть канальцев расположена по экватору тромбоцита, другие можно обнаружить среди органелл. Они не контактируют с плазматической мембраной тромбоцитов, органеллами и системой открытых каналов. Плотная тубулярная система тромбоцитов подобна эндоплазматическому ретикулуму скелетной мышцы [3, 6].
При воздействии агрегантов на тромбоциты они изменяют форму от дисковидной до сферической, образуют псевдоподии и принимают неправильную форму. Организованное концентрическое кольцо микротрубочек распадается. Изменяется распределение микрофиламентов и микротрубочек, имеет место образование клубков из микротрубочек. Физические изменения структуры цитоскелета ассоциированы с выбросом химических веществ из цитоплазмы тромбоцитов во внеклеточную среду [7].
Кровяным пластинкам принадлежит ведущая роль в первичной остановке кровотечений из микрососудов. In vivo тромбоциты циркулируют в кровотоке, практически не взаимодействуя друг с другом, другими клетками крови и эндотелием сосудов. В случае повреждения кровеносного сосуда тромбоциты подвергаются действию различных веществ, инициирующих процессы агрегации (склеивание тромбоцитов друг с другом) и адгезии (прилипание клеток к поврежденной поверхности), в результате которых образуется тромбоцитарная пробка. Наибольший интерес с точки зрения тромбоцитарного гемостаза представляет механизм агрегации тромбоцитов [5].
В случае взаимодействия индуктора с рецептором на поверхности тромбоцитов развивается агрегация тромбоцитов. Процессу агрегации тромбоцитов с образованием агрегатов, предшествует стадия их активации- изменение формы от дисковидной до сферической и образование псевдоподий. Именно в таких преобразованных формах тромбоциты взаимодействуют друг с другом, формируют агрегаты и выбрасывают содержимое гранул [2].
При воздействии на тромбоциты сильных индукторов (например, тромбина) агрегация клеток происходит с большой скоростью и носит, как правило, необратимый характер [4].
Очевидно, имеет место несколько путей активации тромбоцитов веществами, вызывающими агрегацию клеток и реакцию высвобождения. Первый путь включает метаболизм арахидоновой кислоты и образование тромбоксана А2, который является ионофором кальция. Второй путь связан с метаболизмом фосфатидилинозитолов и образованием фосфатидной кислоты, также являющейся ионофором кальция. Третий путь, возможно, обусловлен высвобождением лизолецитинового компонента фосфолипидов плазматической мембраны тромбоцитов, назы ваемого фактором активации тромбоцитов. Предполагают, что ФАТ может активировать тромбоциты независимо от высвобождения Са 2+ [3]. Существенная роль отводится также механизмам активации цАМФ, контролирующего уровень ионов Са 2+ в цитоплазме [6].
Изменение формы тромбоцитов, образование псевдоподий, взаимодействие их друг с другом и реакция высвобождения происходят с участием гликопротеидов и сократительных белков тромбоцитов, активность которых регулируется ионами Са 2+ [5].
Несмотря на то, что молодой возраст является периодом оптимального функционирования всех систем организма, он не свободен от возможности возникновения патологии гемостаза [2, 4, 5]. Возникающие в молодом возрасте отклонения гомеостаза способны нарушать тромбоцитарные функции [1]. К числу таких состояний относится избыточная масса тела и повышение артериального давления, однако, несмотря на накопленную информацию о тромбоцитах, их функциональное состояние у молодых людей с данными отклонениями изучено недостаточно. Не определена степень активности функций тромбоцитов у молодых людей, ведущих малоподвижный образ жизни и регулярно тренирующихся физически, не найдены основные механизмы, обеспечивающие формирование тромбоцитопатии при избыточной массе тела и тенденции к повышению артериального давления.
1. Баркаган Л.З. Рациональная диагностика и контролируемая терапия нарушений гемостаза у детей // Педиатрия.- 1983.-№3.-С.64-66.
4. Левицкая С.В., Баркаган Л.З., Чупрова А.В., Серебряный В.Л. Тромбофилии у детей. М., 1989.
7. Шиффман Ф.Дж. Патофизиология крови. Пер. с англ.-М.-СПб.: «Издательство БИНОМ»- «Невский диалект», 2000.-448с., ил.