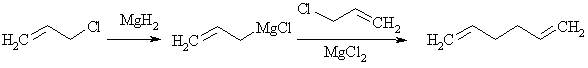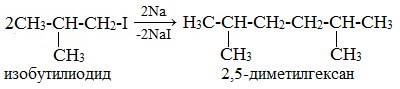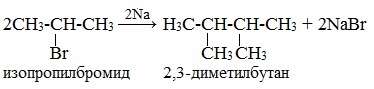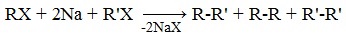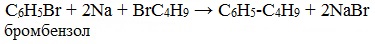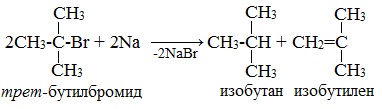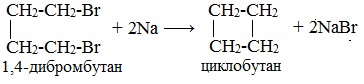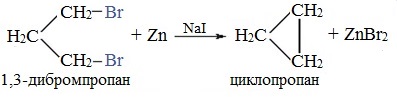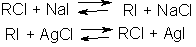Алкилгалогениды с натрием что образуется
Алкилгалогениды. Реакции нуклеофильного замещения.
Реакции элиминирования
Реакции присоединения к галогеналкенам
Галогеналкенам свойственны реакции присоединения, которые протекают по тем же закономерностям, что и в алкенах. Присоединение несимметричных электрофилов подчиняется правилу Марковникова.
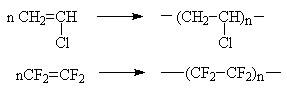
Непредельные галогенопроизводные играют большую роль в производстве полимерных материалов. В результате полимеризации хлористого винила получают поливинилхлорид, перфторалкены являются мономерами фторопластов, важнейшим из которых является тефлон (2).
Взаимодействие с металлами
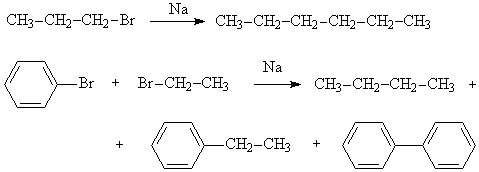
Взаимодействие галогеналканов с металлическим натрием протекает бурно с выделением большого количества тепла. Продуктом реакции является алкан с более длинной углеродной цепью. Сшивание алкильных остатков происходит за счет тех атомов углерода, которые в исходных соединениях были связаны с атомом галогена (реакция Вюрца). Реакция применяется для синтеза углеводородов, причем наилучшие результаты достигаются при использовании одного галогенопроизводного. В противном случае образуется смесь продуктов.
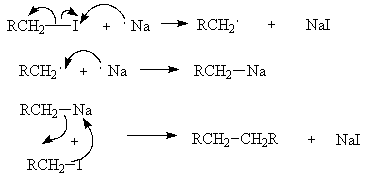
Считают, что начальные стадии реакции имеют свободнорадикальный механизм: натрий отдает один электрон галогену (одноэлектронный перенос), который объединяет с ним один из своих электронов. В результате образуется галогенид натрия и углеводородный радикал, который, присоединив атом натрия превращается в натрийорганическое соединение. Последнее в силу своей высокой активности реагирует с исходным галогенопроизводным. В целом же реакция Вюрца может рассматриваться как нуклеофильное замещение: галогеналкан – субстрат, алкилнатрий – нуклеофил.
Менее активный магний образует более устойчивые, хотя и весьма реакционноспособные, смешанные магнийорганические соединения, называемые реактивами Гриньяра. Они могут вступать в реакцию Вюрца лишь в том случае, когда применяют активный галогеналкан, типа аллилхлорида.
Алкилгалогениды с натрием что образуется
Ацетилениды натрия используются для синтеза высших алкинов, например
Ион ацетиленида атакует атом углерода, при этом происходит замещение иона галогена на ацетиленид-ион и образуется алкин
Поскольку ацетиленид натрия представляет собой соль очень слабой кислоты, ацетилена, ион ацетиленида является очень сильным основанием — фактически более сильным, чем ион гидроксила. При обсуждении синтеза алкенов из алкилгалогенидов (разд. 5.14) было показано, что основной ион гидроксила отщепляет ион водорода, т. е. вызывает элиминирование. И не удивительно, что еще более основной ион ацетиленида также дает продукт элиминирования.
Ион ацетиленида может реагировать с алкилгалогенидом по двум направлениям: атакуя углерод (реакция замещения) или атакуя водород (реакция элиминирования). Показано (разд. 5.15), что реакционная способность алкилгалогенидов в реакции элиминирования уменьшается в следующем порядке: третичный 



в реакцию элиминирования и медленнее в реакцию замещения, в данных условиях дают исключительно алкены.
Если атакующий реагент — сильное основание, такое, как гидроксил- или ацетиленид-ион, т. е. когда реагент имеет большую склонность к иону водорода, реакция элиминирования особенно важна. Практически, только первичные галогениды дают хорошие выходы продукта замещения алкина. Со вторичными и третичными галогенидами элиминирование преобладает настолько, что этот метод нельзя использовать для синтеза соответствующих замещенных алкинов. При изучении органической химии мы будем вновь и вновь возвращаться к конкурирующим реакциям замещения и элиминирования.
Алкилгалогениды с натрием что образуется
Реакция Вюрца — конденсация алкилгалогенидов под действием Na (реже — Li или К) с образованием предельных углеводородов.
Реакция Вюрца — метод синтеза симметричных насыщенных углеводородов действием металлического натрия на алкилгалогениды (галогеналканы).
Легче реакция происходит с алкилиодидами и алкилбромидами, труднее – с алкилхлоридами.
В результате образуется алкан с более сложной углеродной цепью.
Реакцию обычно проводят в диэтиловом эфире.
В процессе реакции Вюрца происходит удвоение углеводородного скелета молекулы и образуется насыщенный углеводород (алкан). Эта реакция находит ограниченное применение, поскольку таким путем можно получать только симметричные алканы.
В основном с ее помощью получают предельные углеводороды с длинной углеродной цепью, особенно она полезна при получении индивидуальных углеводородов большой молекулярной массы (например, гептаконтана C70H142).
Реакцию используют для получения углеводородов с четным числом С-атомов. Если ввести в реакцию два различных галогеналкана, то образуется смесь трех продуктов.
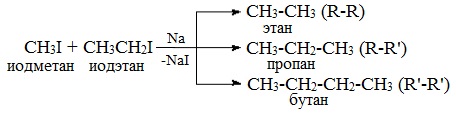
Например, при взаимодействии метил- и этилиодидов с натрием наряду с пропаном образуется этан и бутан:
Эта реакция была открыта французким химиком Ш. Вюрцем в 1855 г. при попытке получения этилнатрия из хлористого этила и металлического натрия.
В 1864г. немецкий химик Р. Фиттиг предложил реакцию, подобную реакции Вюрца, для синтеза жирноароматических углеводородов (реакция Вюрца-Фиттига).
Реакция Вюрца используется для первичных алкилгалогенидов. Для вторичных алкилгалогенидов не имеет практического значения, т.к выход целевого продукта составляет всего 10-15%.
Реакцию Вюрца невозможно использовать для третичных алкилгалогенидов, т.к. вместо алкана с удвоенным числом атомов углерода образуется смесь алкана и алкена с исходным углеродным скелетом.
Внутримолекулярная реакция Вюрца
Реакция Вюрца успешно применяется для внутримолекулярных конденсаций. Этим путем можно получать циклоалканы заданного строения.
При взаимодействии 1,4-дибромбутана с металлическим натрием можно получить циклобутан:
Из 1,3-дибромпропана под действием металлического цинка и йодида натрия, как активатора, может быть получен циклопропан:
При взаимодействии галогеналкилов с металлическим натрием образуются алканы с удвоенным числом углеродных атомов:
6. Получение магнийорганических соединений.
При действии на алкилгалогениды магния в среде абсолютного эфира образуются магнийорганические соединения, называемые реактивами Гриньяра, например: эфир
7. Реакции с алкоголятами
При взаимодействии алкилгалогенидов с алкоголятами образуются простые эфиры:
бромистый этилат диэтиловый
При этом возможно образование непредельных углеводородов.
8. Взаимодействие с аммиаком и аминами
Продуктами реакции являются первичные, вторичные или третичные амины, а также соли аммониевых оснований:
9. Взаимодействие с солями синильной кислоты
Тем самым можно перейти от предельных углеводородов к карбоновым кислотам.
10. Взаимодействие с солями органических кислот:
ацетат серебра этиловый эфир уксусной
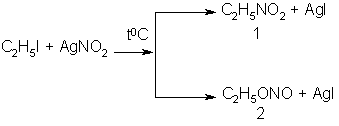
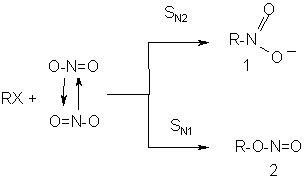
11. Реакции с нитритом серебра:
Механизм и направление реакции зависят от природы растворителя. Так, сольватирующие растворители (вода, спирты) способствуют образованию эфира.
12. Взаимодействие с металлами
При действии на галогенопроизводные многих металлов (двухкратный избыток) галоген замещается металлом. Это важный метод синтеза металлорганических соединений:
6. Отдельные представители
Чтобы распечатать файл, скачайте его (в формате Word).
Гидрирование или восстановление алкилгалогенидов
При каталитическом гидрировании в присутствии палладия алкилгалогениды превращаются в алканы.
Алканы также получают восстановлением алкилгалогенидов металлом в кислоте.
Иодалканы могут быть легко восстановлены в запаянной ампуле с иодистоводородной кислотой.
Реакция галогеналканов с натрием (реакция Вюрца)
Реакция Вюрца позволяет получить углеводород с большим числом атомов углерода, чем в исходном соединении.
Она пригодна для синтеза только симметричных алканов с использованием первичных(!) алкилгалогенидов. В случае использования в качестве исходных соединений различных галогеналканов в результате реакции получается смесь трех углеводородов:
Эту смесь приходится разделять, что не всегда возможно.
Вместо натрия в этой реакции могут быть использованы и другие металлы, например магний, цинк, литий.
Электролиз натриевых или калиевых солей карбоновых кислот приводит также к получению симметричных углеводородов.
Алкены
Геометрические изомеры (состав и способ связывания атомов одинаков, расположение групп и атомов в пространстве различно). Для названия этих изомеров используется Е, Z-номенклатура. При этом возможно использование классических цис-и транс-обозначений для определения пространственного расположения одинаковых или сходных групп относительно плоскости сравнения.
| Одинаковые по старшинству группы расположены по разные стороны от плоскости двойной связи. В этом соединении два метильных радикала находятся в цис-положении. | Одинаковые по старшинству группы расположены по одну сторону от плоскости двойной связи. В этом соединении два метильных радикала находятся в транс-положении. |
Химические свойства
Реакция электрофильного присоединения протекает в две стадии:
По такому механизму протекает реакция присоединения галогеноводородов НСl, НВr, НI. Порядок увеличения реакционной способности галогеноводородов по отношению к алкенам совпадает с порядком увеличения их кислотности: НСl
Присоединению хлора и брома, молекулы которых неполярны, предшествует поляризация
Частицы, присоединяющиеся в медленной и быстрой стадиях электрофильного присоединения, приведены в таблице 2.1.
Реакции электрофильного присоединения
Электрофильное присоединение к алкенам происходит через стадию образования более устойчивого карбокатиона (правило Марковникова). Ряд устойчивости карбокатионов: