Амписид (1.5 г)
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Порошок для приготовления раствора для инъекций 0,75 г, 1,5 г в комплекте с растворителем (0,5 % раствор лидокаина гидрохлорида 1,8 мл, 3,5 мл)
Состав
Для дозировки 0,75 г
Один флакон содержит
активные вещества – ампициллина натрия 531,5 мг (в пересчете на ампициллин – 500 мг) и сульбактама натрия 273,5 мг (в пересчете на сульбактам – 250 мг)
0,5 % раствор лидокаина гидрохлорида 1,8 мл
Для дозировки 1,5 г
Один флакон содержит
активные вещества – ампициллина натрия 1063 мг (в пересчете на ампициллин – 1000 мг) и сульбактама натрия 547 мг (в пересчете на сульбактам – 500 мг)
0,5 % раствор лидокаина гидрохлорида 3,5 мл
Oписание
Белый или почти белый порошок с характерным запахом.
Фармакотерапевтическая группа
Антибактериальные препараты для системного применения. Бета-лактамные антибактериальные препараты. Пенициллины в комбинации с ингибиторами бета-лактамаз.
Фармакологические свойства
Фармакокинетика
Препарат не всасывается в пищеварительном тракте. Ампициллин и сульбактам обладают сходными фармакокинетическими характеристиками. После внутримышечного или внутривенного введения их комбинации достигаются высокие концентрации обоих антибиотиков в сыворотке крови. Период полувыведения обоих ингредиентов составляет приблизительно один час. Ампициллин и сульбактам хорошо распределяются в большинстве тканей и биологических жидкостях организма. Степень проникновения препарата в спинномозговую жидкость низкая, однако она повышается при наличии воспаления мягких оболочек головного мозга.
Большая часть ампициллина и сульбактама (75 %) выводится в неизмененном виде с мочой.
Фармакокинетика у детей
У детей в возрасте 1 года и старше фармакокинетические характеристики препарата аналогичны таковым у взрослых. У новорожденных и недоношенных детей (вероятно, вследствие незрелости функции почек в течение первых дней жизни) период полувыведения обоих действующих веществ увеличен и в среднем составляет 7,9 часа для сульбактама и 9,4 часа для ампициллина. Этим пациентам препарат следует вводить в виде двух равных доз каждые 12 часов, в соответствии со стандартной методикой применения ампициллина.
Фармакокинетика у пациентов с нарушением функции почек
У больных с выраженной почечной недостаточностью (клиренс креатинина
ИНСТРУКЦИЯ
по медицинскому применению препарата
Регистрационный номер: П N014013/04-011009
Торговое название препарата: Амписид
Международное непатентованное название (МНН): сультамициллин
Лекарственная форма: Таблетки, покрытые пленочной оболочкой; порошок для приготовления суспензии для приема внутрь.
Состав:
Таблетки:
Активное вещество: сультамициллина тозилат (в пересчете на сультамициллин) 375 мг.
Вспомогательные вещества: карбоксиметил крахмал натрия, магния стеарат, целлюлоза микрокристаллическая.
Оболочка: гипромеллоза, титана диокисид, макрогол 400.
Порошок для приготовления суспензии для приема внутрь:
Активное вещество: сультамициллин 250 мг / 5 мл.
Вспомогательные вещества: сахароза, камедь ксантановая, гипролоза, кармеллоза натрия, уксусной кислоты ангидрид, натрия дигидрофосфат, ароматизатор «гуарана».
Описание:
Таблетки: белые или белые с желтоватым оттенком таблетки в форме капсул, покрытые пленочной оболочкой, с риской на обеих сторонах; на изломе однородная масса белого или почти белого цвета.
Порошок для приготовления суспензии для приема внутрь: белый или почти белый порошок; готовая суспензия белого или почти белого цвета, однородная.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Антибактериальным компонентом препарата является ампициллин — антибиотик из группы полусинтетических пенициллинов, который обладает бактерицидным действием на чувствительные микроорганизмы во время фазы активного размножения путем угнетения биосинтеза мукопептида клеточной стенки. Сульбактам не обладает клинически значимой антибактериальной активностью (исключение составляют Neisseriaceae и Acinetobacter), он является необратимым ингибитором большинства основных бета-лактамаз, которые продуцируются микроорганизмами, устойчивыми к бета-лактамным антибиотикам. Сульбактам связывается также с некоторыми пенициллинсвязывающими белками, поэтому некоторые штаммы более чувствительны к комбинации, чем к одному бета-лактамному антибиотику.
Амписид активен в отношении широкого спектра грамположительных и грамотрицательных бактерий, включая Staphylococcus aureus и Staphylococcus epidermidis (в том числе пенициллин-резистентные и некоторые метициллинрезистентные штаммы); Streptococcus pneumoniae, Streptococcus faecalis и другие стрептококки, Haemophilus influenzae и Haemophilus parainfluenzae (штаммы, продуцирующие и не продуцирующие бета-лактамазы), Branhamella catarrhalis, Escherichia coli, Klebsiella spp., Proteus spp. (индолположительные и индолотрицательные), Morganella morganii, Citrobacter spp. и Enterobacter spp., Neisseria meningitidis и Neisseria gonorrhoeae; анаэробы, в том числе Bacteroides fragilis, Peptococcus spp., Peptostreptococcus spp. и близкие к нему виды.
Фармакокинетика
Амписид хорошо всасывается при приеме внутрь, не разрушаясь в кислой среде желудка.
Проникает в большинство тканей и биологических жидкостей организма. Плохо проникает через гематоэнцефалический барьер. Выводится преимущественно почками, причем в моче создаются очень высокие концентрации неизмененного антибиотика, а также с желчью и грудным молоком.
Амписид при повторных введениях не кумулирует, что дает возможность применять его длительно в больших дозах.
Показания к применению
Инфекционно-воспалительные заболевания, вызванные чувствительными микроорганизмами: инфекции верхних, нижних дыхательных путей и ЛOP-органов (в том числе синусит, средний отит и эпиглоттит, бактериальные пневмонии); инфекции мочевыводящих и половых органов (в том числе пиелонефрит, эндометрит, цистит, уретрит); инфекции желчевыводящих путей (холецистит, холангит); инфекции кожи, мягких тканей; инфекции костей и суставов; гонококковые инфекции.
Противопоказания
Повышенная чувствительность к ампициллину и сульбактаму и другим бета-лактамным антибиотикам, инфекционный мононуклеоз, лимфолейкоз, тяжелые нарушения функции печени и почек, детский возраст до 3-х лет (при применении таблеток).
Применение при беременности и кормлении грудью
При необходимости применения при беременности следует оценить предполагаемую пользу для матери и потенциальный риск для плода.
При необходимости применения в период лактации следует прекратить грудное вскармливание.
Способ приготовления суспензии
Суспензия приготавливается непосредственно перед первым применением.
Порошок следует растворить кипяченой водой, охлажденной до комнатной температуры, постепенно встряхивая и добавляя воду до метки на флаконе. Затем дать постоять около 5 мин, чтобы обеспечить полное растворение. Флакон следует хорошо встряхивать перед каждым использованием. Для точной дозировки препарата следует использовать мерную ложку, которую нужно хорошо споласкивать водой после каждого употребления. После разведения суспензию следует хранить не более 14 дней в холодильнике, но не замораживать.
Передозировка
Симптомы, возникающие при передозировке препарата, существенно отличаются от его побочных эффектов. Следует учитывать, что высокие концентрации бета-лактамных антибиотиков в спинномозговой жидкости, могут вызывать нарушение функции центральной нервной системы, включая судороги. Как ампициллин, так и сульбактам удаляются из системы кровообращения с помощью гемодиализа.
Лечение: промывание желудка, симптоматическая терапия, гемодиализ (особенно у пациентов с нарушением функции почек).
Взаимодействие с другими лекарственными препаратами
Антикоагулянты: пенициллины могут изменять агрегацию тромбоцитов и показатели гемокоагуляции (усиливают действие антикоагулянтов).
Препараты, обладающие бактериостатическим действием (хлорамфеникол, эритромицин, сульфаниламидные препараты и тетрациклины): антагонистическое действие.
Бактерицидные антибиотики: (в т.ч. аминогликозиды, цефалоспорины, циклосерин, ванкомицин, рифампицин) оказывают синергидное действие.
Антациды, глюкозамин, слабительные лекарственные средства, пища, аминогликозиды (при энтеральном назначении) замедляют и снижают абсорбцию: аскорбиновая кислота повышает абсорбцию.
Пероральные контрацептивы, содержащие эстроген: уменьшает эффективность пероральных контрацептивов, лекарственных средств, в процессе метаболизма которых образуется парааминобензойная кислота, и этинилэстрадиола (риск развития кровотечений «прорыва»).
Метотрексат: совместное назначение пенициллинов приводило к снижению клиренса метотрексата и к возрастанию его токсичности. Подобных пациентов следует тщательно наблюдать.
Пробенецид, диуретики, аллопуринол, фенилбутазон, нестероидные противовоспалительные средства и др. препараты, снижающие канальцевую секрецию, повышают концентрацию ампициллина и сульбактама в плазме, приводят к более длительному их сохранению в крови, удлинению периода полувыведения и возрастанию риска токсичности.
Влияние на лабораторные показатели: неферментативные методы определения сахара в моче, с использованием реактивов Бенедикта, Фелинга или Клинитеста могут дать ложноположительный результат. Отмечалось, что применение ампициллина у беременных женщин приводило к преходящему снижению в плазме крови уровней общего связанного эстриола, эстриол-глюкоронида, а также связанного эстрона и эстрадиола.
Аллопуринил: повышает риск развития кожной сыпи.
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 375 мг: 10 таблеток во флакон оранжевого стекла тип III, завинчивающийся алюминиевой или пластмассовой крышкой. Во флакон помещают пластиковый цилиндрический контейнер с осушителем (силикагель) по размеру, отличающийся от таблеток, либо контейнер с осушителем встраивают в крышку флакона (является частью уплотнителя).
1 флакон в картонную пачку с инструкцией по применению.
200 флаконов (2000 таблеток) в картонную коробку (для стационаров) с равным количеством инструкций по применению.
Порошок для приготовления суспензии для приема внутрь 250 мг/5 мл: во флаконы по 40 мл или 70 мл желтого стекла типа III с риской, укупоренный алюминиевой крышкой.
1 флакон в картонную пачку вместе с мерной ложкой и инструкцией по применению. 100 флаконов с инструкциями по применению в картонную коробку (для стационаров).
Срок годности
2 года. Не использовать препарат после истечения срока годности.
Условия хранения
Таблетки: при температуре не выше 25°С, в сухом, защищенном от света месте.
Хранить в недоступном для детей месте.
Порошок для приготовления суспензии для приема внутрь:
при температуре не выше 25°С, в сухом, защищенном от света месте.
Хранить в недоступном для детей месте.
После растворения препарат сохраняет активность в течение 14 дней при температуре хранения 2-8°С.
Условия отпуска из аптек
По рецепту.
Производитель:
«Мустафа Невзат Илач Санаи А.Ш.», Турция.
Пак иш Меркези, проф. Др. Булент, Таркан Сокак № 5/1, 34349 Гайреттепе, Стамбул, Турция
Дистрибьютор:
ООО «АСФАРМА-РОС»,
г.Казань
Особенности антибактериальной терапии у недоношенных новорожденных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Научный центр здоровья детей РАМН, Москва
И нфекционно-воспалительные заболевания – наиболее частая патология у детей периода новорожденности, что объясняется своеобразием защитных механизмов на данном этапе онтогенеза. Наиболее выражена недостаточность гуморального и клеточного иммунитета, незрелость барьерных функций кожи и слизистых у детей, родившихся преждевременно. В структуре диагнозов в отделениях второго этапа выхаживания недоношеных детей удельный вес гнойно-воспалительных заболеваний приближается к 80%, при этом большинство заболеваний составляют так называемые малые инфекции – гнойничковые сыпи, омфалит, дакриоцистит, отит; у 1% детей выявляются серьезные воспалительные заболевания (флегмона и пузырчатка новорожденных, остеомиелит, менингоэнцефалит, пневмония, сепсис).
В последние годы проблемы инфекционной патологии у незрелых детей приобрели особую актуальность в связи с изменением особенностей как макро-, так и микроорганизмов, что отразилось на течении инфекционного процесса. Утяжелилось течение фоновых состояний, создающих благоприятную почву для манифестации и прогрессирования инфекции – это перинатальные поражения мозга, врожденные пороки развития, пневмопатии; причем достижения современной реаниматологии и интенсивной терапии позволяют обеспечить выживание даже детей с крайне малой массой тела, перенесших тяжелую асфиксию. В свою очередь реанимационные мероприятия, прежде всего длительная ИВЛ и катетеризация магистральных сосудов, создают условия для микробной агрессии. Одним из важных факторов, способствующих бактериальной контаминации и утяжелению течения бактериальных инфекций, является наличие смешанной вирусно-бактериальной внутриутробной инфекции. Внутриутробные паразитарные и вирусные инфекции (так называемый TORCH-синдром) в 13–45% случаев являются основной причиной смертности в периоде новорожденности. Перенесенная внутриутробно специфическая инфекция резко нарушает защитные механизмы ребенка, что способствует присоединению и бурному течению интранатальных и постнатальных бактериальных инфекций.
Современная этиология возбудителей
В этиологической структуре возбудителей бактериальных инфекций у недоношенных детей 10–15 лет назад отмечалось увеличение удельного веса грамотрицательной флоры (клебсиела, протей, псевдомонас). Однако в последующие годы вновь среди этиологических агентов локальных гнойно-воспалительных поражений первое место занимает грамположительная флора (стафилококки, стрептококки). Для недоношенных детей характерны сочетание микроорганизмов, выделяемых из различных очагов (например, из гнойного очага высеваются золотистый и эпидермальный стафилококки, из кала – кишечная палочка и стафилококки), а также смена ведущих возбудителей в процессе лечения (первоначальные агенты воспаления подавляются, их место занимают другие бактерии, часто в сочетании с грибами).
Среди населения циркулируют преимущественно чувствительные к антибиотикам штаммы возбудителей (В.К.Таточенко), а в стационарах дети обсеменяются преимущественно устойчивыми штаммами (внутрибольничная флора), так как условно-патогенные и сапрофитные микроорганизмы многократно пассируются на ослабленных незрелых новорожденных и происходит их селекция под воздействием терапии (Г.В.Яцык, И.В.Маркова). Кроме того, устойчивые штаммы (клебсиеллы, стрептококк В) передаются новорожденным от больных матерей.
Специфика фармакокинетики антибиотиков
У новорожденных детей фармакокинетика любого препарата существенно отличается от таковой у детей более старшего возраста; в наибольшей мере это относится к незрелым (недоношенным) новорожденным. Крайне важной представляется незрелость выделительной функции почек и ферментных систем печени – эти особенности в первую очередь характерны для глубоконедоношенных детей с массой тела менее 1500 г. Помимо этого, незрелость других органов и систем (желудочно-кишечного тракта, нервной системы, органов дыхания), а также общая лабильность метаболизма накладывают на фармакокинетику антибиотиков у недоношенных детей индивидуальные особенности предопределяя высокий риск нежелательных побочных эффектов антибактериальной терапии. Общая особенность фармакокинетики любых препаратов у недоношенных детей – это ее замедление, что способствует кумуляции лекарств и влияет на выбор дозы (уменьшение ее на 1/3–1/4), путей и кратности введения препаратов. В то же время повышенная проницаемость естественных барьеров (кожи и слизистых) способствует всасыванию многих медикаментов. В настоящее время проводятся исследования суточных ритмов фармакодинамики различных препаратов, но в отношении антибиотиков у недоношенных детей таких исследований практически нет.
Показания и выбор антибиотика
Безусловным показанием для назначения антибиотикотерапии недоношенному новорожденному является наличие у него любого инфекционно-воспалительного процесса, включая так называемые малые инфекции, например, нераспространенные гнойничковые поражения кожи, гнойные конъюнктивиты, отиты (в том числе катаральный отит). Лишь в редких случаях легкого течения неосложненной ОРВИ (ринофарингит) антибиотик не назначается – и то только у детей с относительно благополучным фоном (незначительная степень недоношенности, отстутствие анамнестических указаний на внутриутробную инфекцию, нетяжелая перинатальная энцефалопатия).
Безусловным показанием для назначения антибиотикотерапии недоношенному новорожденному является наличие у него любого инфекционно-воспалительного процесса, включая так называемые малые инфекции, например, нераспространенные гнойничковые поражения кожи, гнойные конъюнктивиты, отиты (в том числе катаральный отит). Лишь в редких случаях легкого течения неосложненной ОРВИ (ринофарингит) антибиотик не назначается – и то только у детей с относительно благополучным фоном (незначительная степень недоношенности, отстутствие анамнестических указаний на внутриутробную инфекцию, нетяжелая перинатальная энцефалопатия).
Спорный вопрос о так называемом профилактическом применении антибиотиков у маловесных недоношенных из группы риска по реализации внутриутробной и интранатальной инфекции (больная мать, длительный безводный период и т.п.), как правило, решается в пользу назначения антибиотика, так же как и в случаях так называемых неинфекционных пневмопатий. К условно “профилактическим” можно отнести также назначение антибиотика для “прикрытия” гормональной кортикостероидной терапии и некоторых вмешательств (катетеризации, переливания крови и т.п.).
Выбор антибиотика для недоношенного ребенка – ответственный момент, во многом определяющий эффективность лечения. При выборе препарата следует учитывать следующие факторы:
• вид возбудителя (в начале лечения часто лишь предполагаемый) и его штамм;
• чувствительность возбудителя (также в начале лечения – предполагаемую, через 2–3 дня после получения результатов бактериологических анализов в терапию могут быть внесены коррективы). В последние годы высказывается мнение о том, что параметры чувствительности микробов in vitro не всегда совпадают с таковыми in vivo и нет необходимости строго следовать им при назначении препаратов;
• локализация и степень тяжести инфекционного процесса (при нетяжелых локальных поражениях возможно пероральное применение препарата; при тяжелых, как правило, – сочетание пероральных и парентеральных средств);
• сопутствующие состояния и премобидный фон (предпочтение парентеральных препаратов при тяжелом дисбактериозе или внутривенного введения у крайне маловесных детей с неразвитой мышечной тканью).
Все антибиотики можно условно разделить на 2 группы – препараты первого выбора назначают, когда нет оснований думать о лекарственной устойчивости флоры (полусинтетические пенициллины, аминогликозиды I поколения, цефалоспорины I поколения); препараты второго выбора направлены на преодоление устойчивых штаммов (аминогликозиды и цефалоспорины III–IV поколения, современные макролиды). Существуют и препараты третьего выбора (или препараты резерва), применяемые при крайне тяжелых формах заболеваний с полирезистентной флорой (карбапенемы).
У недоношенных детей в основном сразу используются препараты второго выбора: применение антибиотиков первого ряда у них неэффективно и лишь способствует отсрочке манифестных проявлений инфекционного процесса, маскирует клинические симптомы. У детей периода новорожденности даже по жизненным показаниям не должны использоваться препараты, обладающие высокой токсичностью (фторхинолоны).
Схема 1. Допустимые сочетания антибиотиков у недоношенных детей при одновременном применении (Г.В. Яцык)
Особенности дозировки антибиотиков
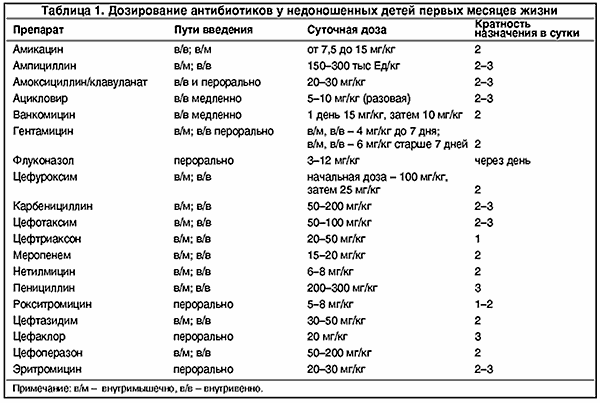
Дозировки используемых в неонатологии антибиотиков для недоношенных детей и кратность их введения представлены в табл. 1 (Г.В. Яцык, 1998 г.) Общий принцип подбора дозы для новорожденного ребенка – большее по сравнению со старшими детьми количество препарата на 1 кг массы тела – сохраняется и у недоношенных детей. Это обусловлено большим процентным содержанием воды в организме новорожденного и большей относительной поверхностью тела.
Дозировки используемых в неонатологии антибиотиков для недоношенных детей и кратность их введения представлены в табл. 1 (Г.В. Яцык, 1998 г.) Общий принцип подбора дозы для новорожденного ребенка – – сохраняется и у недоношенных детей. Это обусловлено большим процентным содержанием воды в организме новорожденного и большей относительной поверхностью тела.
Комбинированная антибактериальная терапия у недоношенных детей должна проводиться с большой осторожностью; одновременное сочетание 2 (очень редко – 3) антибиотиков применяется лишь у детей с тяжелыми гнойно-воспалительными процессами (прежде всего при сепсисе), вызванными смешанной флорой. Допустимые сочетания антибиотиков представлены в табл. 2 и на схеме 1 (данные Н.В. Белобородовой).
Пути и кратность введения антибиотиков недоношенному ребенку
В связи с высокой проницаемостью и ранимостью слизистой желудочно-кишечного тракта у незрелых новорожденных, а также опасностью развития дисбиоза и язвенно-некротического энтероколита пероральные антибиотики использовались ограниченно. К тому же большинство инфекционных заболеваний у недоношенных детей по тяжести состояния требует более мощной терапии. В последние годы появились достаточно действенные антибактериальные и противогрибковые препараты для перорального применения (макролиды, амоксициллин/клавуланат и др.) Кроме того, установлено крайне негативное воздействие болевых раздражений на грудных детей, что делает необходимым ограничение внутримышечных и внутривенных инъекций.
У новорожденных (особенно недоношенных) детей период полувыведения препаратов увеличен вследствие незрелости почек и печени. Поэтому кратность введения большинства препаратов не превышает у них 2 раз в течение суток (за исключением пенициллинов); особенно популярными в неонатологии остаются препараты пролонгированного действия (рокситромицин, цефтриаксон), допускающие однократное применение. Некоторые исследователи (Н.В. Белобородова, О.Б. Ладодо) большинство парентеральных препаратов (в том числе аминогликозиды, цефалоспорины) предлагают вводить однократно – внутривенно или внутримышечно.
Продолжительность антибактериальной терапии и последовательность применяемых антибиотиков у недоношенного ребенка определяются индивидуально, они зависят от эффективности первичного курса антибактериальной терапии, которая оценивается по традиционным клиническим и лабораторным параметрам. Как правило, недоношенным детям со среднетяжелыми инфекционными процессами (омфалит, пневмония, отит и т.д.) проводят два последовательных курса антибиотика (второй курс с учетом чувствительности микрофлоры), каждый по 7–10 дней. При тяжелых заболеваниях (менингит, остеомиелит, сепсис) обычно используют не менее 3–4 курсов антибиотиков (или 2–3 курса; при первом – сочетание антибиотиков, обычно аминогликозида и цефалоспорина III–IV поколения).
Побочные явления и их профилактика
Наиболее распространенные у недоношенных новорожденных нежелательные побочные эффекты антибактериальной терапии обусловлены подавлением симбионтной микрофлоры и, как следствие, колонизацией организма условно-патогенными сапрофитами. В связи с этим даже после короткого курса антибактериальной терапии у недоношенных детей возможно развитие дисбиозов – кандидоза кожи и слизистых, кишечного дисбактериоза. Реже у недоношенных отмечаются токсические (по типу идиосинкразии) и аллергические реакции на антибиотики.
Профилактика осложнений антибактериальной терапии начинается уже с ее правильного подбора, тщательного индивидуального контроля. Одновременно с назначением антибиотиков ребенку необходимо назначать противогрибковые средства (леворин, флуконазол, амфотерицин В) и средства, восстанавливающие микрофлору кишечника (бифидум-бактерин и др.); причем использование последних продолжается не менее недели после окончания курса антибиотиков.
С целью снижения нагрузки антибиотиками на незрелый организм недоношенного ребенка в последние годы делаются попытки сочетания антибактериальной терапии со средствами, усиливающими неспецифическую защиту: иммуноглобулинами, лазеротерапией (использование низкоинтенсивного лазерного излучения на магистральные сосуды с целью иммуностимуляции), метаболитной коррекцией.