Доказать что фермент может обратимо и необратимо инактивироваться
Исследовательские работы и проекты
Необратимое и обратимое ингибирование
Ингибирование
Необратимое ингибирование наблюдают в случае образования ковалентных стабильных связей между молекулой ингибитора и фермента. Чаще всего модификации подвергается активный центр фермента. В результате фермент не может выполнять каталитическую функцию.
К необратимым ингибиторам относят ионы тяжёлых металлов, например ртути (Hg2+), серебра (Ag+) и мышьяка (As3+), которые в малых концентрациях блокируют сульфгидрильные группы активного центра. Субстрат при этом не может подвергаться химическому превращению.
Конкурентное ингибирование. Использование конкурентных ингибиторов в медицине
К конкурентному ингибированию относят обратимое снижение скорости ферментативной реакции, вызванное ингибитором, связывающимся с активным центром фермента и препятствующим образованию фермент-субстратного комплекса.
Такой тип ингибирования наблюдают, когда ингибитор – структурный аналог субстрата, в результате возникает конкуренция молекул субстрата и ингибитора за место в активном центре фермента. В этом случае с ферментом взаимодействует либо субстрат, либо ингибитор, образуя комплексы фермент-субстрат (ES) или фермент-ингибитор (EI). При формировании комплекса фермента и ингибитора (EI) продукт реакции не образуется.
Классический пример конкурентного ингибирования – ингибирование сукцинатдегидрогеназной реакции малоновой кислотой. Малоновая кислота – структурный аналог сукцината (наличие двух карбоксильных групп) и может также взаимодействовать с активным центром сукцинатдегидрогеназы. Однако отщепление двух атомов водорода от малоновой кислоты невозможно; следовательно, скорость реакции снижается.
Многие лекарственные препараты оказывают своё терапевтическое действие по механизму конкурентного ингибирования. Например, четвертичные аммониевые основания ингибируют ацетилхолинэстеразу, катализирующую реакцию гидролиза ацетилхолина на холин и уксусную кислоту.
При добавлении ингибиторов активность ацетилхолинэстеразы уменьшается, концентрация ацетилхолина (субстрата) увеличивается, что сопровождается усилением проведения нервного импульса. Ингибиторы холинэстеразы используют при лечении мышечных дистрофий. Эффективные антихолинэстеразные препараты – прозерин, эндрофоний и др [3].
Изоферменты. Значение изоферментов в медицине
Наличие множественных форм ферментов, или изоферментов, установлено более чем для 100 ферментов, выделенных из различных видов животных, растений и микроорганизмов. Изоферменты не всегда состоят из двух или нескольких субъединиц. У ряда ферментов отдельные изофермсаты представляют собой разные по химическому строению белки, обладающие одной и той же каталитической активностью, но состоящие только из одной субъединицы.
Медицинское значение. Активность ЛДГ в плазме крови повышается при острых поражениях сердца, печени, почек и др. органов, а также при различных анемиях. Диагностическое значение имеет определение не суммарной активности всех типов ЛДГ, а изоферментов, так как только они являются органоспецифичными. Например, при инфаркте миокарда в крови резко возрастает ЛДГ1, при гепатитах – ЛДГ5 [5].
Ферментативные цепи. Регуляция ферментативных цепей. Ключевые ферменты
Регуляция в ферментативных цепях направлена на ключевые ферменты, которые катализируют, как правило, необратимые реакции.
Использование ферментов в медицине
Ферменты используются в лёгкой, пищевой, микробиологической, фармацевтической промышленности, а также в генноинженерных исследованиях и биотехнологии. Успехи энзимологии находят всё большее применение в медицине.
Медицинская энзимология – новое направление энзимологии, которая имеет свои цели и задачи, специфические методологические подходы и методы исследований.
1. Энзимодиагностика, которая в свою очередь развивается по двум путям:
2. Изучение таких болезней, причина которых лежит в отсутствии или недостаточности тех или иных ферментов – энзимопатологии или энзимопатии.
3. Энзимотерапия – использование ферментов и регуляторов активности ферментов в качестве лекарственных препаратов[5].
Разница между Обратимым и Необратимым ингибированием ферментов
Обратимое и необратимое ингибирование фермента — это два метода механизма ингибирования фермента, ответственных за снижение активности фермента. И нгибиторы снижают совместимость субстрата и фермента, что приводит к ингибированию образования фермент-субстратных комплексов.
Содержание
Что такое Обратимое ингибирование фермента
Существуют несколько типов обратимых ингибиторов ферментов, которые являются конкурентными, неконкурентными, бесконкурентными а также смешанными ингибиторами. Из них конкурентными ингибиторами являются соединения, имеющие структурное сходство с субстратом определенного фермента. Следовательно, он конкурирует с субстратом за достижение активного центра фермента, снижая ферментативное действие. Напротив, неконкурентные ингибиторы связываются с ферментом или комплексом фермент-субстрат в месте, отличном от активного центра. Тем не менее, это может изменить 3D-конформацию фермента, что, в свою очередь, снижает функцию фермента.
В свою очередь бесконкурентные ингибиторы связываются с комплексом фермент-субстрат, эффективно устраняя комплекс фермент-субстрат и, таким образом, уменьшая образование продукта. С другой стороны, смешанные ингибиторы могут связываться как с ферментом, так и с комплексом фермент-субстрат, высвобождая субстрат из образующего комплекса фермент-субстрат-ингибитор. В отличие от смешанных ингибиторов, неконкурентные ингибиторы не допускают диссоциации субстрата от образующегося комплекса фермент-субстрат-ингибитор.
Конкурентное и бесонкурентное ингибирование ферментов
Что такое Необратимое ингибирование фермента?
Пример необратимого ингибирования ферментов в лекарственном препарате можно увидеть в Аспирине
Например, нервные газы, особенно DIFP, необратимо ингибируют биологические системы, образуя комплекс фермент-ингибитор. Обычно это происходит через определенную группу ОН серина в активных центрах определенных ферментов. Как правило, пептидазы, такие как трипсин и химотрипсин, содержат сериновые группы в активном центре, которые могут ингибироваться DIFP. Следовательно, этот тип ковалентных модификаций активного центра фермента может привести к постоянной инактивации фермента, и ферментативное действие трудно восстановить путем добавления избытка субстрата в среду.
Сходство между Обратимым и Необратимым ингибированием фермента
Разница между Обратимым и Необратимым ингибированием фермента
Обратимое ингибирование фермента относится к процессу связывания ингибиторов с ферментом посредством нековалентных взаимодействий, так что после удаления они позволяют восстановить функцию фермента. Между тем, необратимое взаимодействие фермента относится к процессу связывания ингибиторов с ферментом посредством ковалентных взаимодействий, так что их диссоциация занимает длительное время, навсегда устраняя действие фермента.
При обратимом ингибировании фермента комплекс фермент-ингибитор быстро диссоциирует, но комплекс фермент-ингибитор очень медленно диссоциирует при необратимом ингибировании фермента.
Обратимое ингибирование фермента может быть восстановлено, но необратимое ингибирование фермента занимает много времени для восстановления.
Типа обратимого ингибирования фермента — это конкурентное, неконкурентное, бесконкурентное и смешанное ингибирование, в то время как необратимое ингибирование фермента происходит посредством ковалентной инактивации активного центра фермента.
Некоторые из примеров обратимых ингибиторов ферментов включают DHFR, противовирусные препараты, такие как ритонавир, осельтамивир и типранавир. Между тем, некоторые примеры необратимых ингибиторов ферментов включают аспирин, дифторметилорнитин, инсектициды, такие как малатион, гербициды, такие как глифосат, и дезинфицирующие средства, такие как триклозан.
Заключение — Обратимое против Необратимого ингибирования ферментов
Обратимое ингибирование фермента — это процесс временного подавления действия фермента. Следовательно, при устранении ингибирующего действия функция фермента может быть восстановлена. Также обратимые ингибиторы связываются с ферментом посредством нековалентных взаимодействий. Следовательно, он позволяет быстро диссоциировать комплекс фермент-ингибитор, восстанавливая функцию фермента. Напротив, необратимое ингибирование фермента представляет собой процесс постоянного ингибирования функции фермента. Следовательно, диссоциация комплекса фермент-ингибитор является продолжительной. Кроме того, молекулы-ингибиторы ковалентно связываются с остатками активного центра фермента, блокируя образование комплекса фермент-субстрат. Основное различие между обратимым и необратимым ингибированием фермента заключается в механизме связывания ингибиторов с ферментом и вытекающих из этого эффектах.
Ингибирование ферментов: обратимое и необратимое; конкурентное и неконкурентное. Лекарственные препараты как ингибиторы ферментов.
Ингибиторы вызывают большой интерес для выяснения механизмов ферментативного катализа, помогают установить роль отдельных ферментов в метаболических путях организма. В основе действия многих лекарственных препаратов и ядов лежит ингибирование активности ферментов, поэтому знание механизмов этого процесса крайне важно для молекулярной фармакологии и токсикологии.
Ингибиторы способны взаимодействовать с ферментами с разной степенью прочности. На основании этого различают обратимое и необратимое ингибирование. По механизму действия ингибиторы подразделяют на конкурентные и неконкурентные.
А. Обратимое ингибирование
Обратимые ингибиторы связываются с ферментом слабыми нековалентными связями и при определённых условиях легко отделяются от фермента. Обратимые ингибиторы бывают конкурентными и неконкурентными.
Конкурентное ингибирование
Для конкурентного типа ингибирования справедливы следующие уравнения:
Кинетические зависимости
Конкурентные ингибиторы уменьшают скорость химической реакции. Конкурентный ингибитор повышает Кm для данного субстрата (уменьшает сродство субстрата к ферменту). Это означает, что в присутствии конкурентного ингибитора необходима большая концентрация субстрата для достижения 1/2 Vmax.
Увеличение соотношения концентрации субстрата и ингибитора снижает степень ингибирования. При значительно более высоких концентрациях субстрата ингибирование полностью
Неконкурентное ингибирование
Неконкурентным называют такое ингибирование ферментативной реакции, при котором ингибитор взаимодействует с ферментом в участке, отличном от активного центра. Неконкурентные ингибиторы не являются структурными аналогами субстрата.
Неконкурентный ингибитор может связываться либо с ферментом, либо с фермент-субстратным комплексом, образуя неактивный комплекс. Присоединение неконкурентного ингибитора вызывает изменение конформации молекулы фермента таким образом, что нарушается взаимодействие субстрата с активным центром фермента, что приводит к снижению скорости ферментативной реакции.
Кинетические зависимости
Этот тип ингибирования характеризуется снижением Vmax ферментативной реакции и уменьшением сродства субстрата к ферменту, т.е. увеличением Кm.
Б. Необратимое ингибирование
Необратимое ингибирование наблюдают в случае образования ковалентных стабильных связей между молекулой ингибитора и фермента. Чаще всего модификации подвергается активный центр фермента, В результате фермент не может выполнять каталитическую функцию.
1. Специфические и неспецифические
ингибиторы
2. Необратимые ингибиторы ферментов как
лекарственные препараты
Аллостерическая регуляция активности ферментов. Роль аллостерических ферментов в метаболизме клетки. Аллостерические эффекторы и ингибиторы. Особенности строения и функционирования аллостерических ферментов и их локализация в метаболических путях. Регуляция активности ферментов по принципу отрицательной обратной связи. Привести примеры.
Активность некоторых аллостерических ферментов стимулируется специфическими активаторами. Аллостерический фермент, регулирующий одну из катаболических последовательностей реакций, может, например, подчиняться стимулирующему влиянию положительных эффекторов – АДР или АМР и ингибирующему действию отрицательного эффектора – АТР. Известны также случаи, когда аллостерический фермент какого-нибудь метаболического пути специфическим образом реагирует на промежуточные или конечные продукты других метаболических путей. Благодаря этому оказывается возможной координация скорости действия различных ферментных систем.
Дата добавления: 2018-02-18 ; просмотров: 5408 ; Мы поможем в написании вашей работы!
Доказать что фермент может обратимо и необратимо инактивироваться
Некоторые вещества вызывают необратимое ингибирование ферментов. Рассмотрим два примера такого рода.
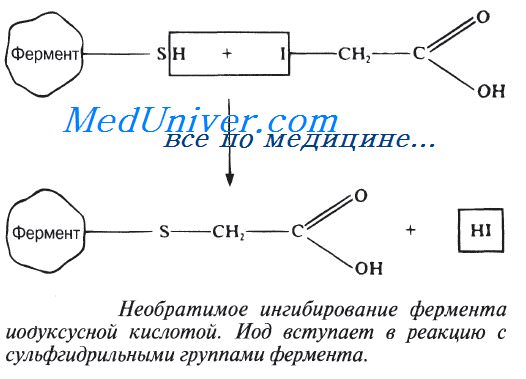
Очень малые концентрации ионов тяжелых металлов, например ионов ртути (Hg2+), серебра (Ag+) и мышьяка (As+), а также определенные иодсодержащие соединения полностью ингибируют некоторые ферменты. Эти вещества необратимо соединяются с сульфгидрильными группами (—SH) в молекуле фермента (рис. 4.13), причем сульфгидрильные группы могут находиться как в активном центре фермента, так и вне его. В любом случае структура фермента нарушается и он теряет способность осуществлять катализ. Может произойти и осаждение ферментного белка.
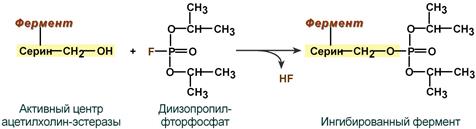
Другой пример необратимого ингибирования — действие диизопропилфторфосфата (ДФФ), соединения из группы нервно-паралитических отравляющих веществ. ДФФ связывается с остатком аминокислоты серина, находящимся в активном центре фермента ацетилхолинэстеразы. Этот фермент инактивирует ацетилхолин, играющий роль нейромедиатора. Одна из функций ацетилхолина заключается в обеспечении передачи нервного импульса от одного нейрона к другому через синаптическую щель.
Аллостерические ферменты
Один из самых обычных способов регуляции метаболических путей — это регуляция с помощью аллостерических ферментов. Аллостерическими называют ферменты, действие которых «по определению» связано с изменением формы (alios — иной, другой; stereos — форма).
Активность таких ферментов регулируют вещества, действующие подобно неконкурентным ингибиторам. Эти вещества присоединяются к ферментам в особых участках, удаленных от активного центра, и меняют активность фермента, вызывая обратимое изменение в структуре активного центра.
В результате меняется и способность субстрата связываться с ферментом (чем данное явление и отличается от неконкурентного ингибирования). Действующие таким образом вещества называются аллостерическими ингибиторами. Рисунок поясняет механизм аллостерического ингибирования.
Примером данного явления служит реакция, протекающая во время гликолиза, который составляет одну из стадий процесса клеточного дыхания. Клеточное дыхание служит источником АТФ. Если концентрация АТФ высока, то АТФ, действуя как аллостерический ингибитор, подавляет активность одного из ферментов гликолиза. Если же клеточный метаболизм усиливается, а следовательно, АТФ расходуется и его общая концентрация падает, то после того как ингибитор будет удален, данный метаболический путь снова вступает в действие. Это может также служить примером ингибирования конечным продуктом.
Лекарства обычно ингибируют ферменты
В медицине активно разрабатываются и используются соединения, изменяющие активность ферментов с целью регуляции скорости метаболических реакций и уменьшения синтеза определенных веществ в организме.
Подавление активности ферментов обычно называют ингибированием, однако это не всегда корректно. Ингибитором называется вещество, вызывающее специфичное снижение активности фермента. Таким образом, неорганические кислоты и тяжелые металлы ингибиторами не являются, а являются инактиваторами, так как снижают активность многих ферментов, т.е. действуют неспецифично.
Ингибирование ферментов
Можно выделить два основных направления ингибирования
Необратимое ингибирование
При необратимом ингибировании происходит связывание или разрушение функциональных групп фермента, необходимых для проявления его активности.
Например, вещество диизопропилфторфосфат прочно и необратимо связывается с гидроксигруппой серина в активном центре фермента ацетилхолинэстеразы, гидролизующей ацетилхолин в нервных синапсах. Ингибирование этого фермента предотвращает распад ацетилхолина в синаптической щели, в результате чего медиатор продолжает оказывать воздействие на свои рецепторы, что бесконтрольно усиливает холинергическую регуляцию.
Аналогично диизопропилфторфосфат ингибирует химотрипсин и другие протеазы, имеющие в активном центре серин (сериновые протеазы).
Диизопропилфторфосфат относится к нервно-паралитическим ядам, аналогичным образом действуют боевые фосфоорганические вещества (зарин, зоман). Сюда же относится вещество «малатион», включенный в инсектициды (карбофос, дихлофос) и превращающийся в организме насекомых в ингибитор ацетилхолинэстеразы, а в организме животных и человека разрушающийся до безвредных продуктов.
Механизм необратимого ингибирования ацетилхолинэстеразы
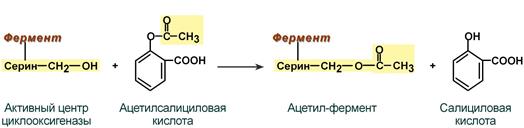
Еще один пример связан с ингибированием ацетилсалициловой кислотой (аспирином) ключевого фермента синтеза простагландинов – циклооксигеназы. Эта кислота входит в состав противовоспалительных средств и используется при воспалительных заболеваниях и лихорадочных состояниях. Присоединение ацетильной группы к гидроксильной группе серина в активном центре фермента вызывает инактивацию последнего и прекращение синтеза простагландинов.
Механизм необратимого ингибирования циклооксигеназы
Третьим показательным примером необратимого ингибирования является влияние антибиотика пенициллина на фермент транспептидазу, сшивающую цепи пептидогликана как последний шаг в синтезе клеточной стенки бактерий.
Обратимое ингибирование
При обратимом ингибировании происходит непрочное связывание ингибитора с функциональными группами фермента, вследствие чего активность фермента постепенно восстанавливается.
Примером обратимого ингибитора может служить прозерин, связывающийся с ферментом ацетилхолинэстеразой в ее активном центре. Группа ингибиторов холинэстеразы (прозерин, дистигмин, галантамин) используется при миастении, после энцефалита, менингита, травм ЦНС.
Конкурентное ингибирование
При таком виде ингибирования ингибитор по своей структуре похож на субстрат фермента. Поэтому он соперничает с субстратом за активный центр (за контактный участок), что приводит к уменьшению связывания субстрата с ферментом и нарушению катализа. В этом состоит особенность конкурентного ингибирования – возможность усилить или ослабить ингибирование через изменение концентрации субстрата. При данном ингибировании максимальная скорость реакции остается вполне достижимой при создании высоких концентраций субстрата.
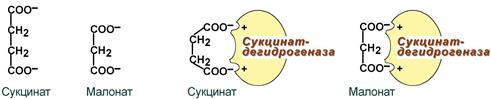
1. Ингибирование фермента цикла трикарбоновых кислот сукцинат-дегидрогеназы малоновой кислотой, структура которой схожа со структурой субстрата этого фермента – янтарной кислоты (сукцината).
Конкурентное ингибирование сукцинатдегидрогеназы
3. В качестве других примеров лекарственных конкурентных ингибиторов можно привести
Данный вид ингибирования связан с присоединением ингибитора не в активном центре, а в другом месте молекулы. Но при этом меняется структура активного центра и связь с субстратом становится невозможной. Это может быть аллостерическое ингибирование, когда активность фермента снижается естественными модуляторами, или связывание с ферментом каких-либо веществ вне активного и аллостерического центра. Например:
Особенностью неконкурентного ингибитора является его способность связываться с ферментом независимо от субстрата, т.е. изменение концентрации субстрата никак не влияет на образование комплекса фермент-ингибитор.
В этом случае ингибитор связывается в активном центре с фермент-субстратным комплексом. Повышение концентрации субстрата, увеличивая количество фермент-субстратного комплекса, усиливает и связывание ингибитора с ним. Таким образом, бесконкурентное ингибирование более сложно, чем другие типы ингибирования.
Смешанное ингибирование
При таком ингибировании ингибитор способен присоединяться везде – не только в активном центре, но и в других частях молекулы. Но после этого фермент еще способен частично сохранять свою активность. Примером является влияние мертиолата (ртутьорганическое вещество) на сахаразу грибов микромицетов для подавления их роста.